تجارب كيميائية ممتعة ورائعة ستشاهدها للمرة الأولى!

7 د
الكيمياء منذ القدم ساعدتنا في مجالات لا حصر لها في الحياة، وقد أخذت بجمالها قلوب العديد من الناس، بدأت بتخمينات بسيطة، وتطورت كثيرا على مر الزمن لتصبح أشبه بالخدع لكن علم لا تخمين فيه.
هنالك من يرى أن الكيمياء مملة ومعقدة، لكن دعونا الآن من هذه الصورة السلبية، ولنحاول تغييرها، ولننتقل إلى شيء أكثر إمتاعا قد لا تصدق أنه يحدث، لنر جمال الكيمياء في اثني عشر تفاعلا من العديد العديد من التفاعلات المدهشة التي تحدث في الحياة، لكن حذار من تجربتها دون الأخذ بقواعد السلامة، ولنبدأ مع شيء قد يكون مألوفاً:
قلب الزئبق النابض:
لا، ليس قلبا قد يضخ الدم، ولا يوجد في أي كائن حي، وليس من خلايا، لكنه قطرة تنبض من الزئبق:
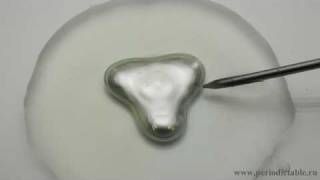

كيف نجعله يرقص ويضطرب بهذا الشكل؟ هذه عملية أكسدة كهروكيماوية، لفعلها نضع قطرة من الزئبق في زجاجة ساعة (صحن زجاجي مقعر قليلا) فوقها محلول من حمض موصل كحمض الكبريتيك مع عامل مؤكسد كبيرمنغنات البوتاسيوم أو فوق أكسيد الهيدروجين (ماء الأكسجين) أو دايكرومات البوتاسيوم، ونقرب منها كما رأينا رأس مسمار من الحديد بحيث يكاد يلامس الزئبق بزاوية مناسبة، هنا يبدأ الزئبق بالنبض والحركة مغيرا شكله.
ما الذي يحصل؟ في المحلول يتأكسد الزئبق بفعل العامل المؤكسد إلى أيون الزئبق، وهذا يقلل من قوى التجاذب بين جزيئات الزئبق (التوتر السطحي) لأن الأيونات ذات الشحنة نفسها تتنافر وتتغلب على القوى بينها، مما يزيد من انتشاره حتى يتلامس مع الحديد، فيتأكسد أيون الحديد محل أيون الزئبق، فيعود الزئبق إلى حالته الطبيعية ذات التوتر السطحي العالي، فيتكور ويبتعد عن الحديد، وتعاد العملية مرات أخرى.
المغنيسيوم والثلج الجاف:
الثلج الجاف هو ثاني أكسيد الكربون في حالة الصلابة، وأظن أن أغلبنا رأى تفاعل احتراق المغنيسيوم بنصوع شديد في تجارب الصفوف الأولى للعلوم أو في الألعاب النارية أو حتى في فلاش الكاميرات القديمة، لكن المغنيسيوم لا يتوقف عند هذا الحد، بل يذهب إلى التفاعل مع ثاني أكسيد الكربون الصلب بنصوع شديد وبوهج برتقالي جميل، محترقا ومنتجا الفحم.
الثلج الحار:
هذه المرة الثلج ليس غازا بل محلول أسيتات الصوديوم المائي فوق المشبع، بمعنى أنه يتبلور أو يترسب الفائض منه إذا تم تحريكه أو إضافة المزيد من المذاب، يتم تحضيره بإذابة كمية من أسيتات الصوديوم في ماء حار حتى يذوب كله، ثم يبرد في الثلاجة فنحصل على محلول فوق الإشباع، يتبلور هذا المحلول بشكل يشبه الثلج؛ لهذا اكتسب اسمه، الجميل في محلول أسيتات الصوديوم هو مقدرتنا على تكوين أشكال جميلة منه عندما يتبلور، فلننظر إلى الفيديو:

الجدير بالذكر أن أسيتات الصوديوم تستخدم في أكياس التدفئة (heating pads) لأنه يصبح حارا عندما يتبلور، كما وأنه يستخدم كمادة لحفظ الطعام.
سفينة تطفو على الهواء:
لا تفرك عينيك! إنها فعلا تطفو فوق الهواء، انه ليس هواءً عاديا بل سداسي فلوريد الكبريت، قد لا تصدقني عندما أقول لك ذلك لكن شاهد الفيديو أولا:

هناك غازات أخف من الهواء كثيرا كالهيليوم، لكن سداسي فلوريد الكبريت أكثر كثافة من الهواء حوالي خمس مرات، لذلك يمكن أن يسكب في الأوعية المفتوحة أو قد تطفو عليه بعض المواد كتلك السفينة المصنوعة من ورق الألمنيوم كما لو كان ماءً. هذا الغاز لا لون له وليس ساما، لكن ماذا يحدث عند استنشاقه؟ يخفض هذا الغاز من طبقة الصوت بشكل ممتع، فيبدو الصوت كأنه صوت رجل آلي عملاق، على عكس تأثير الهيليوم، واللذان نشاهدهما هنا:

يعود هذا التأثير إلى أن الهيليوم أخف من الهواء فيخرج من الرئتين سريعا مما يرفع من طبقة الصوت والعكس صحيح لسداسي فلوريد الكبريت والذي يخرج بطيئا مما يخفض طبقة الصوت.
أنا أكره الحلوى!
لا أظن أن أحدا يكره الحلوى لكن يبدو أن مصهور كلورات البوتاسيوم ليس على علاقة جيدة بأي شيء يلامسه أثناء حالة انصهاره، كقطعة الحلوى هذه:

تستخدم كلورات البوتاسيوم كمطهر وأيضا في الألعاب النارية والمتفجرات، إذ انه عندما يسخن إلى انصهاره ينزعج من أي شيء يضاف إليه ويؤدي ذلك إلى انحلاله على شكل انفجار، لكنه يطلق غاز الأكسجين، فلهذا يستعمل أحيانا كمصدر للأكسجين في الطائرات والغواصات ومحطات الفضاء، المشكلة في الأمر أنه أنتج حريقا في أحد محطات مير الفضائية بسبب تفاعله هذا.
اللعب في مواجهة النيتروجين السائل:
النيتروجين والذي يشكل أربع أخماس الهواء الجوي لديه أحد أقل درجات التجمد والغليان – يتجمد عند درجة -210 م، ويغلي عند درجة -196 م، لذا يستخدم النيتروجين السائل في التبريد، وكما الغازات الأخرى يتمدد النيتروجين عند ارتفاع درجة الحرارة، وهذا ما أدى إلى انفجاره أو توليد حركة في التجارب التالية:
بطيخة في مواجهة النيتروجين السائل:

في البركة:
كرة التنس:

تأثير ميسنر (Meissner effect)، ابتعد عني!
رأينا تأثير البرودة الشديدة على البطيخة والمسبح وكرة التنس النفاثة، لكن ما تأثير البرودة الشديدة على الموصلات؟ عندما نبرد مادة فائقة الموصلية (مقاومتها النسبية = صفر في حالات خاصة، فتصبح موصلاً تاماً) إلى ما دون درجة حرارتها الحرجة، تظهر خصائصها فائقة التوصيل وينتج مجال مغناطيسي معاكس أي لا يجذب الفلزات كما يجذبها المغناطيس، بل ينفرها عن مجاله ولا يجعلها تقترب منه. تخيل استخدام هذه الخاصية في النقل بدون الاحتكاك، فتطفو المواد على السكة بدلا من استخدام العجلات، كم هذا مدهش، أليس كذلك؟ قد لا تصدق لكن صورة خير من ألف كلمة:

تفاعل إشارة المرور:
قد تحزرون لماذا سمي هذا التفاعل بهذا الاسم.. لا، فهو لا ينظم حركة المرور، بل بسبب أنه يمر بمرحلة خضراء، ثم حمراء لكنها سرعان ما تصبح صفراء. يتم تفاعل إشارة المرور بأكسدة أو اختزال صبغة نيلية اللون اسمها (Indigo carmine)، ويتم استخدام محلول الغلوكوز أو الدكستروز (سكر العنب أو سكر الذرة) مع محلول هيدروكسيد الصوديوم أو البوتاسيوم مضافا إليهما الصبغة.
أجمل ما في الأمر أنه يمكن عكس التفاعل وإعادته إلى اللون الأخضر ليبدأ من جديد عبر خض الزجاجة الموجود فيها المحلول عدة مرات أو سكب المحلول في وعاء آخر أو إضافة ماء الأكسجين إليه.


كيف يحدث هذا؟ يقوم سكر الغلوكوز بخزل الصبغة النيلية فيتحول لونها إلى الأخضر ثم تدريجيا حتى الأحمر فالأصفر، لكن عند خض الزجاجة أو سكبها أو إضافة ماء الأكسجين إليها، يتخللها الأكسجين ويقوم بأكسدة الصبغة لتعود إلى لونها الأخضر.
تفاعل الثيرمايت: لا يقهر..
تفاعل الثيرمايت كان –من شدة حرارته– التفاعل المستخدم في لحام السكك الحديدية قديما، انه تفاعل بودرة الألمنيوم (أو معادن أخرى لكنه الأشد والأفضل في الألمنيوم) مع أكسيد معدن آخر خاصة أكسيد الحديد (صدأ الحديد) مطلقاً طاقة هائلة قادرة حتى على صهر الحديد، ويحتاج التفاعل كي يبدأ إلى شرارة قادح ومع أنه غير متفجر إلا أنه يرشق نارا وينتج حرارة عاليه لزمن قصير، فلا يقدر حتى النيتروجين السائل على تهدئة فورته.
الهيليوم فائق السيولة:
تعرفون غاز الهيليوم الخفيف، فقد تحدثنا عن تأثيره كغاز قبل قليل، لكن ماذا عنه كسائل؟ يصل الهيليوم إلى درجة الغليان عند درجة حرارة 4,22 كلفن (-268,93 ْم) ويكون له خصائص السائل العادية ويسمى هيليوم I، لكن عند وصوله إلى ما دون درجة لامدا 2,1768 كلفن (-270,97 ْم) يتحول إلى هيليوم II، وهي حالة السيولة الفائقة (superfluid)، يبدأ يخالف السوائل بجنون فيتسلق جدران الوعاء الموجود فيه، وتصبح لزوجته صفرا عندما يمر في أنابيب دقيقة جدا (قطرها من10-7 إلى 10-8 متر)

التفاعل المتردد: تفاعل بريغز– راوشر (Briggs–Rauscher)
يتردد هذا التفاعل بشكل مذهل ما بين الشفافية واللون البرتقالي ويتحول فجائيا إلى اللون الكحلي، ثم يتلاشى هذا اللون تلقائيا وتدريجيا إلى اللون الشفاف لتعاد الكرة، كما في الفيديو:

هذا التفاعل هو أحد التفاعلات القليلة والنادرة والتي تتردد بهذا الشكل، طبعا لن يستمر هكذا للأبد، بل يتوقف بعد حوالي عشر تحولات حسب المواد المضافة إليه وينتهي به الأمر بعد نفاد مخزون المواد فيه إلى اللون الكحلي فائحة منه رائحة اليود مصدر هذا اللون. هل هذا سحر؟ بالطبع لا، يحدث هنا تفاعلان يتحكمان في بعضهما: تفاعل أول سريع يحدث في ظروف معينة وهو المسؤول عن التحول الفجائي إلى اللون الكحلي.
كما يطلق مواد كيميائية تحفز التفاعل الثاني البطيء على الحدوث، والتفاعل الآخر البطيء والذي يعيد اللون الكحلي إلى اللون الشفاف، وهو يطلق مواد كيميائية تبطل من التفاعل الأول لكن سرعان ما يتم امتصاصها بواسطة مادة مضافة إلى التفاعل، فتوفر الظروف الملائمة للتفاعل الأول لكي يعاد حدوثه، وتعاد الكرة حتى نفاد المخزون.
في النهاية أتمنى أن تكونوا قد استمتعتم بهذه التفاعلات المثيرة، وإن استطعتم أن تفعلوا بعضا منها أو رأيتم أن هناك تفاعلات أخرى تستحق المشاهدة فيمكنكم مشاركتها معنا.
عبَّر عن رأيك
إحرص أن يكون تعليقك موضوعيّاً ومفيداً، حافظ على سُمعتكَ الرقميَّةواحترم الكاتب والأعضاء والقُرّاء.
 ذكاء اصطناعي
ذكاء اصطناعي أجهزة ذكية
أجهزة ذكية ريادة
ريادة أعظم الكتب
أعظم الكتب هواتف
هواتف توب التوب
توب التوب منصات
منصات عملات رقمية
عملات رقمية